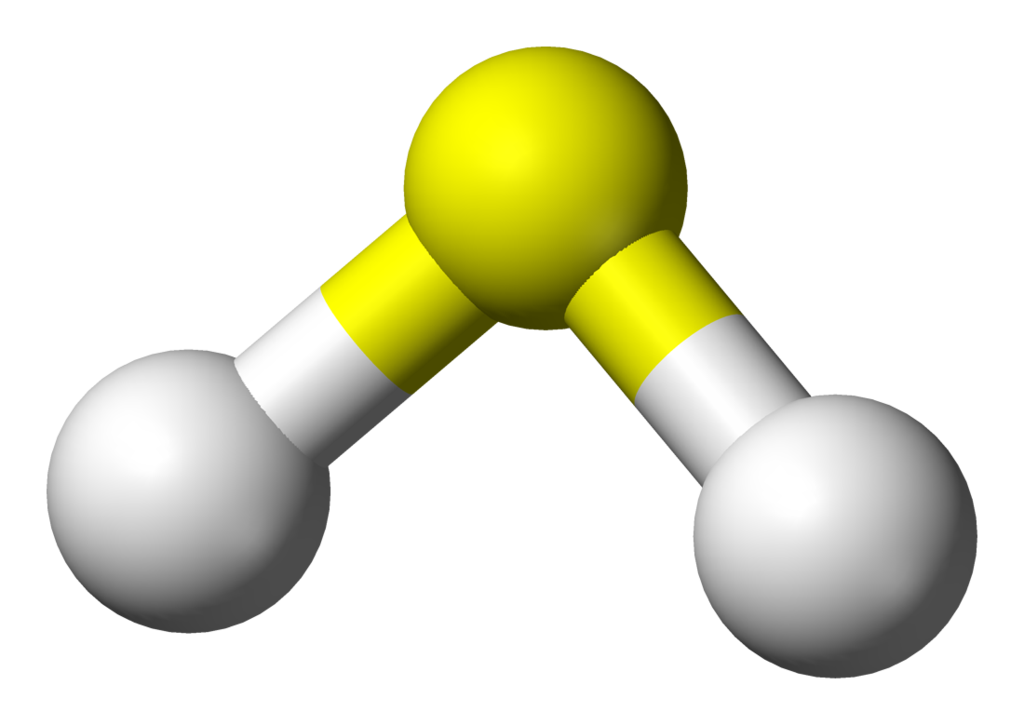
Siarczki są solami bardzo słabego kwasu siarkowodorowego. Siarkowodór jest gazem silnie trującym, w małym stopniu rozpuszczalnym w wodzie; jest on kwasem tak słabym, że jego sole hydrolizują w wodzie z wydzieleniem siarkowodoru. Siarkowodór i jony siarczkowe są silnymi reduktorami. Większkość metali tworzy siarczki trudno rozpuszczalne w wodzie.