
Próba płomieniowa
Na K Ca Sr Ba Li Rb Cs Cu B Pb Sn As Sb Bi
Próba płomieniowa, czyli barwienie płomienia palnika gazowego jest przykładem wykorzystania zjawiska emisji promieniowania w analizie jakościowej.
Metoda emisyjnej spektroskopii atomowej polega na badaniu charakterystycznego promieniowania emitowanego przez atomy pierwiastków po ich wzbudzeniu w odpowiedniej temperaturze.
W wysokiej temperaturze związki niektórych metali wyparowują, a ich pary pobudzone do świecenia zabarwiają płomień palnika w charakterystyczny dla siebie sposób. Każdy pierwiastek posiada swoje unikalne widmo emisyjne:
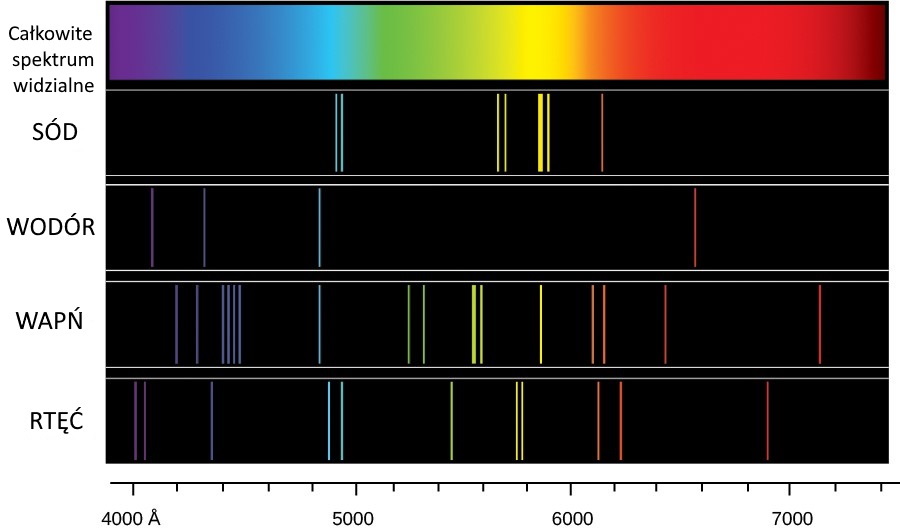 Zabarwienie to jest efektem wzbudzenia elektronów atomów metali w płomieniu, które wracając do stanu podstawowego emitują kwant światła o ściśle określonej długości fali. Warto zaznaczyć, że jony litowców np. Na+, nie posiadają elektronu walencyjnego. Elektron znajdujący się na powłoce n-1 nie może być wzbudzony zbyt małą energią płomienia palnika. Z tego powodu jon sodu w pierwszej kolejności ulega rekombinacji z wolnym elektronem, a dopiero potem może dojść do wzbudzenia i relaksacji, której towarzyszy emisja m.in. żółtego światła o długości fali równej 589 nm - tzw. linia D sodu. Różnica pomiędzy poziomami 3s i 3p to 2.1 eV, która ze wzoru:
Zabarwienie to jest efektem wzbudzenia elektronów atomów metali w płomieniu, które wracając do stanu podstawowego emitują kwant światła o ściśle określonej długości fali. Warto zaznaczyć, że jony litowców np. Na+, nie posiadają elektronu walencyjnego. Elektron znajdujący się na powłoce n-1 nie może być wzbudzony zbyt małą energią płomienia palnika. Z tego powodu jon sodu w pierwszej kolejności ulega rekombinacji z wolnym elektronem, a dopiero potem może dojść do wzbudzenia i relaksacji, której towarzyszy emisja m.in. żółtego światła o długości fali równej 589 nm - tzw. linia D sodu. Różnica pomiędzy poziomami 3s i 3p to 2.1 eV, która ze wzoru: (gdzie E to energia fotonu, h to stała Plancka, λ to długość fali światła, c to prędkość światła w próżni) odpowiada długości fali 589nm.

Sposób postrzegania długości fali elektromagnetycznej jako kolor przez ludzki mózg jest bardzo złożona. Fala o długości 589nm jest postrzegana jako kolor żółty, 650nm jako czerwony, a 450nm jako niebieski. Natomiast nie ma jednej fali elektromagnetycznej, która jednoznacznie odwzorowywałaby różowy, ponieważ, jest to kolor powstający przy połączeniu niebieskiego i czerwonego - kolorów po przeciwnych stronach spektrum światła widzialnego. Ta strona symuluje odbieraną barwę na podstawie wybranej długości fali.
Nie należy badać w płomieniu, na druciku platynowym, roztworów zawierających metale ciężkie, ponieważ metale te wtapiają się w platynę. Można wtedy użyć drutu z innego metalu np. drutu niklowo-chromowego. Do tego doświadczenia najlepiej używać drucika platynowego kilkakrotnie oczyszczonego przez zanurzenie w kwasie solnym i wyprażonego w nieświecącym płomieniu palnika gazowego.



