- Oranż metylowy
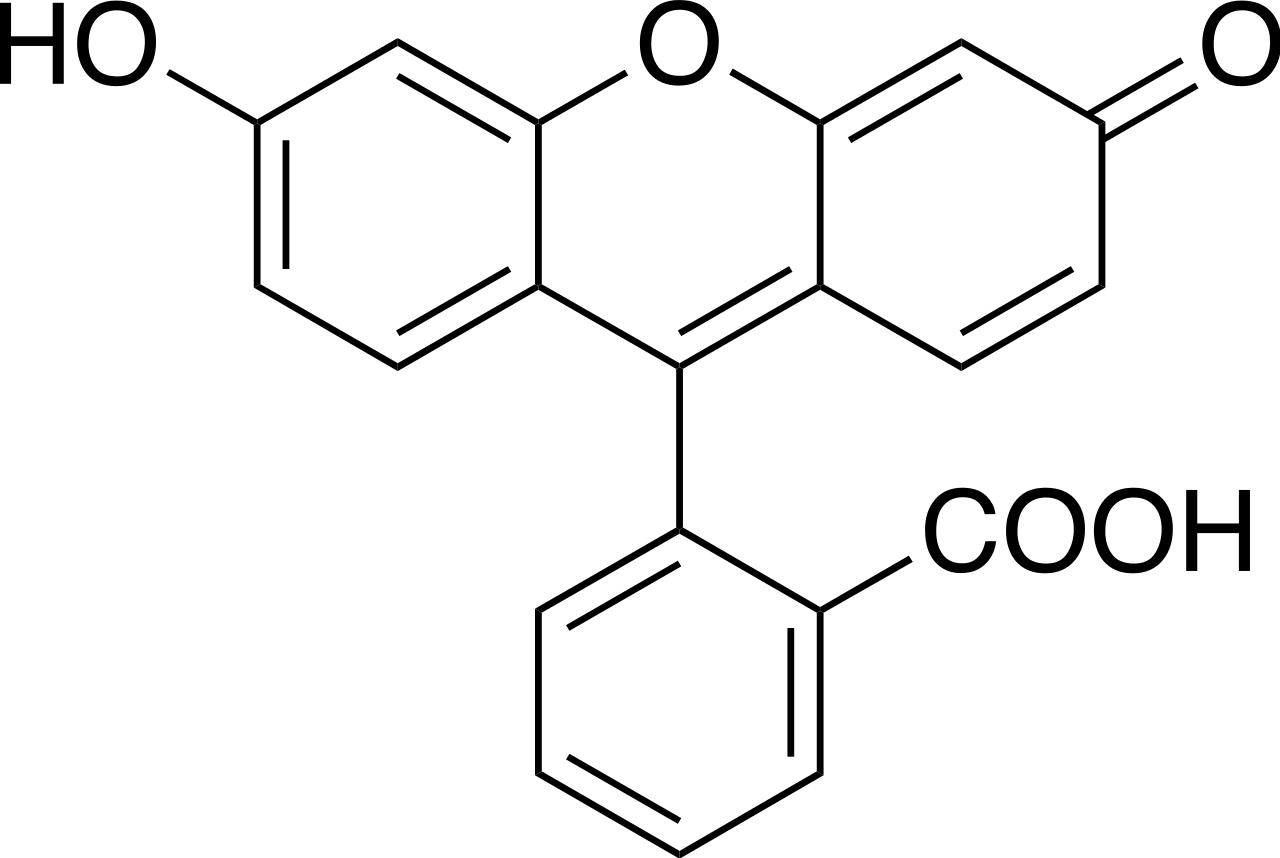
- Fluoresceina
- Fenoloftaleina
- Tymoloftaleina
- Czerwień metylowa
- Czerwień fenolowa
- Czerwień bromofenolowa
- Błękit tymolowy
Fluoresceina jest ciemnoczerwonym proszkiem, słabo rozpuszczalnym w wodzie i w alkoholach. W roztworach o odczynie zasadowym wykazuje silną zielonożółtą fluorescencję. Fluoresceina absorbuje maksymalnie światło o λ=494 nm i emituje maksymalnie λ=521 nm (w wodzie). pKa = 6.4